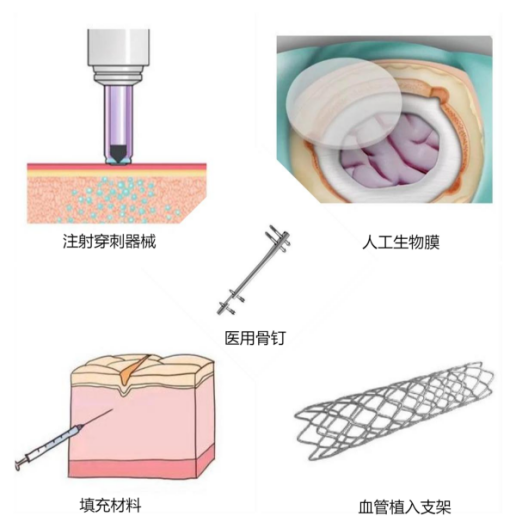
汇智泰康为介入式创新医疗器械产品成械性研究提供全面技术支持
2022-06-15发表创新药物、国产高端医疗器械、先进诊疗技术让人民群众享受到更多高质量的创新成果。科技创新有力支撑了高质量发展,医疗器械行业也在发展浪潮中闯出一条新路。根据数据统计,在2017-2021年间,不管是医疗器械高新技术企业的数量,还是进入及获批国家级创新医疗器械审评的产品数量,整体都呈现稳步上升趋势。
创新医疗器械产品最终可以产品化,过程中很重要的一步就是进行成械性研究。汇智泰康依托配置齐全的毒理学安全评价平台、分析仪器平台和经验丰富的技术团队,基于AAALAC、GLP、计量认证(CMA)等认证资质,可以为客户提供全面的成械性生物学性能技术服务和合规申报服务等。服务对象主要是Ⅲ类医疗器械,即用于植入人体、支持、维持生命;对人体具有潜在危险,对其安全性、有效性必须严格控制的医疗器械。
汇智泰康医疗器械成械性研究服务项目的典型代表包括:
1)各种载药支架和球囊医疗器械的动物植入试验,包括小型猪、犬、兔子等的植入试验及植入后的毒理学、病理学和伴随毒代的样品采集工作;
2)各种生物基质样品的取材及生物基质样品含量分析工作,包括载药紫杉醇、他克莫司、雷帕霉素、三氧化二砷等的含量检测;
3)神经鞘管类的可降解材料的评价研究,包括动物实验的手术植入、术后定期观察、行为学方面的影响判断等试验工作;
4)可降解的镁锌合金支架、替代关节和可降解的骨钉等材料进行的药代、慢性毒性以及伴随毒代研究的样品含量分析工作等。
以上服务项目涉及的多种属的动物,汇智泰康均有实验动物的许可资质;样品检测使用的各种分析仪器,主要包括LC-MS/MS,GC-MS/MS,ICP-MS,以及毒理研究所需要的组织病理和临床病理的各种分析仪器等,汇智泰康均配套齐全。
介入式创新医疗器械产品成械性研究,汇智泰康可以提供以下几个方面的服务:- SPF清洁级动物房搭配使用,满足不同试验要求
- 医疗器械生物学评价(试验依据:GB/T16886)
- 组织病理研究服务
- 临床病理服务
- 医疗器械及生物医学材料成分、组织与结构分析
- 生物学评价生物样品分析
- 其它技术咨询服务
详细信息请点击下方链接:
汇智泰康医疗器械生物学评价技术服务平台 (iphasepharma.com)
创新药物、国产高端医疗器械、先进诊疗技术让人民群众享受到更多高质量的创新成果。科技创新有力支撑了高质量发展,医疗器械行业也在发展浪潮中闯出一条新路。根据数据统计,在2017-2021年间,不管是医疗器械高新技术企业的数量,还是进入及获批国家级创新医疗器械审评的产品数量,整体都呈现稳步上升趋势。
创新医疗器械产品最终可以产品化,过程中很重要的一步就是进行成械性研究。汇智泰康依托配置齐全的毒理学安全评价平台、分析仪器平台和经验丰富的技术团队,基于AAALAC、GLP、计量认证(CMA)等认证资质,可以为客户提供全面的成械性生物学性能技术服务和合规申报服务等。服务对象主要是Ⅲ类医疗器械,即用于植入人体、支持、维持生命;对人体具有潜在危险,对其安全性、有效性必须严格控制的医疗器械。
汇智泰康医疗器械成械性研究服务项目的典型代表包括:
1)各种载药支架和球囊医疗器械的动物植入试验,包括小型猪、犬、兔子等的植入试验及植入后的毒理学、病理学和伴随毒代的样品采集工作;
2)各种生物基质样品的取材及生物基质样品含量分析工作,包括载药紫杉醇、他克莫司、雷帕霉素、三氧化二砷等的含量检测;
3)神经鞘管类的可降解材料的评价研究,包括动物实验的手术植入、术后定期观察、行为学方面的影响判断等试验工作;
4)可降解的镁锌合金支架、替代关节和可降解的骨钉等材料进行的药代、慢性毒性以及伴随毒代研究的样品含量分析工作等。
以上服务项目涉及的多种属的动物,汇智泰康均有实验动物的许可资质;样品检测使用的各种分析仪器,主要包括LC-MS/MS,GC-MS/MS,ICP-MS,以及毒理研究所需要的组织病理和临床病理的各种分析仪器等,汇智泰康均配套齐全。
介入式创新医疗器械产品成械性研究,汇智泰康可以提供以下几个方面的服务:- SPF清洁级动物房搭配使用,满足不同试验要求
- 医疗器械生物学评价(试验依据:GB/T16886)
- 组织病理研究服务
- 临床病理服务
- 医疗器械及生物医学材料成分、组织与结构分析
- 生物学评价生物样品分析
- 其它技术咨询服务
详细信息请点击下方链接:
汇智泰康医疗器械生物学评价技术服务平台 (iphasepharma.com)